医疗器械作为关乎人民健康和生命安全的特殊产品,其质量和安全备受关注。通过UDI实现对医疗器械产品的有效追溯监管也逐渐成为一项稳步推进的工作内容。
什么是UDI
UDI是医疗器械唯一标识(unique device identification)的简称,是医疗器械产品的电子身份证。在医疗器械产品或者包装上附载的,由数字、字母或符号组成的代码,用于对医疗器械进行唯一性识别。可以实现医疗器械标识和各项产品数据的记录,并确认产品的生产企业、型号、规格等属性信息。

UDI
UDI的申请流程
1.确定UDI实施的产品范围和注册人/备案人:根据国家药监局发布的相关通告和文件要求,明确哪些产品需要实施UDI。
2.申请厂商识别代码:企业需要加入GS1系统,申请UDI-DI厂商识别代码。申请可以通过线上(如中国物品编码中心网站)或线下(到当地编码分支机构)进行。
3.分发产品标识:将全球贸易项目编号(GTIN)分配给医疗器械的最小销售单元以及较高包装或医疗器械产品。确保GTIN以14位数字存在于数据库中。
4.发放生产标识:生产标识(PI)应根据监管和实际应用需要确定,可能包括医疗器械序列号、生产日期等内容。
5.UDI标签生成:完成GTIN分配和确定PI后,生成UDI标签。UDI应包括机器可读码(如一维码或二维码)和人工可读的数字字母组合。
6.UDI数据上传:在申请医疗器械注册、注册变更或办理备案时,在注册/备案管理系统中提交UDI-DI。在销售产品前,确保产品标识和相关数据上传至中国医疗器械唯一标识数据库(UDID)。
7.关联医保数据:对于已在医保局数据库中维护信息的医疗器械,需要在UDI数据库中补充完善医保医用耗材分类与代码字段,并确认数据一致性。
8.维护数据:注册人/备案人应负责维护UDI数据库中的数据,确保数据的真实性、准确性和完整性。当产品标识相关数据发生变化时,应在产品上市销售前进行数据更新。
9.标签打印与检测:企业可通过UDI服务平台进行UDI标识的制作,并在生产完成后完成UDI编码的打印,附在产品包装上。对条码印制质量等进行检测,确保UDI的可读性。
10.建立程序文件:建议注册人/备案人建立相关程序文件,确保UDI管理过程规范化、制度化。
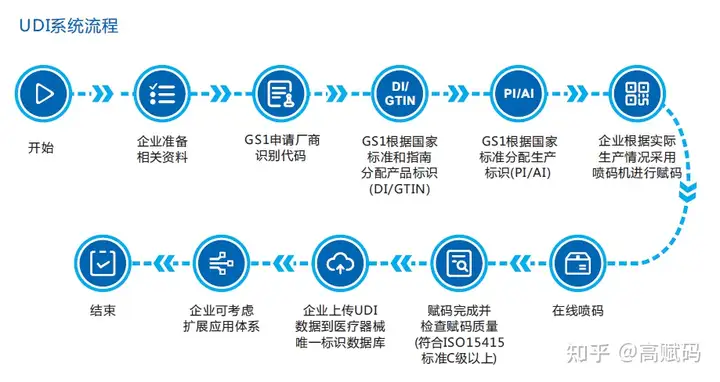
UDI系统流程
UDI在医疗器械中的意义
1.提高信息透明度:通过公开UDI信息,可以提高医疗信息的透明度,方便公众了解医疗器械的相关信息。患者可以通过查询UDI了解医疗器械的详细信息,包括生产商、产品规格、使用说明等。这有助于增强公众对医疗器械的信任和使用信心。
2.加强质量控制:UDI可以用于生产过程中的质量控制。通过记录每个产品的生产过程和关键参数,可以方便地对产品质量进行追溯和分析。如果发现质量问题,可以迅速找到问题根源并采取措施加以解决。
3.提高管理效率:通过UDI,医疗器械制造商可以快速、准确地识别和追踪产品,从而提高管理效率。在遇到问题时,制造商可以迅速确定问题产品的位置和批次,避免问题产品的扩散和损失的扩大。
4.优化物流管理:通过UDI,医疗器械可以在供应链中实现准确、快速的识别和追踪。这有助于优化物流管理,提高运输效率并降低成本。同时,UDI还可以帮助医疗机构在库存管理中实现精细化管理,避免库存积压和浪费。
UDI可以实现医疗器械的追踪、管控和召回,以及医疗设备的识别和分类。同时,医疗机构可以通过UDI在全球范围内查找和比较不同厂家的产品,提高采购效率和准确性。




